Tartalom
- szakaszában
- 1. módszer Elemezze a reakció sebességét
- 2. módszer Ábrázolja az adatok grafikonját
- 3. módszer Kísérletileg oldja meg a problémát
Gyakran elengedhetetlen annak ismerete, hogy a vegyi anyagok koncentrációja hogyan befolyásolja a reakció sebességét, hogy megértsük a különféle kémiai folyamatokat. A "reakció sorrendje" arról szól, hogy egy vagy több reagens koncentrációja hogyan változtatja meg a reakció sebességét. A kémiai reakció általános sorrendje az összes jelen lévő reagens reakció sorrendjének összege. Nem elegendő, ha megfigyeli a reakció egyensúlyi egyenletét a sorrend meghatározásához, de ezt az információt levonhatja a reakció sebességéből vagy az azt ábrázoló grafikonból.
szakaszában
1. módszer Elemezze a reakció sebességét
-

Elemezze a sebesség egyenletét. A reakciósebesség-egyenlet segít meghatározni a reakció sorrendjét. Ez az egyenlet arra szolgál, hogy kiemelje az egyik kémiai anyag növekedését vagy csökkenését az eltelt idő függvényében. A reakcióhoz kapcsolódó bármely más típusú egyenlet nem teszi lehetővé a reakció sorrendjének azonosítását. -

Azonosítsa a reagensek sorrendjét. A sebesség-egyenletben szereplő reagensek kitevője 0, 1 vagy 2 (rendkívül ritka, ha 2-nél nagyobb exponensekkel találkozunk). Csak annyit kell tennie, hogy fontolja meg ennek a kiállítónak az értékét, aki elmondja az egyes reagensek sorrendjét.- Ha az exponens nulla, akkor a kérdéses reagens koncentrációja nem befolyásolja a reakció sebességét.
- Ha a kitevő értéke 1, ez azt jelenti, hogy az érintett reagens koncentrációjának növelése lineárisan növeli a reakció sebességét (ha megkétszerezi a koncentrációját, megkétszerezi a reakció sebességét).
- Ha az exponens 2, akkor a reakció sebessége négyszögletesen növekszik a reagens koncentrációjának növelésével (ha megkétszerezzük a koncentrációt, a sebesség szorozva 4-del).
- Legtöbbször, mivel a nulla teljesítményre emelkedett szám mindig 1 lesz, a nulla rendű reagenseket nem említik a sebesség-egyenletekben.
-

Adja hozzá az összes reagens sorrendjét. A kémiai reakció általános sorrendje az egyes reagensek rendjeinek összege. Tehát csak az összes reagens kitevőit kell összeadnia, hogy meg tudja határozni a kémiai reakció sorrendjét. Általában ez az eredmény 2-nél kisebb vagy azzal egyenlő.- Például, ha az első számú reagens elsőrendű (azaz 1-es exponenssel rendelkezik), és a második számú reagens szintén elsőrendű (az 1-es exponenssel is rendelkezik), akkor a teljes reakció másodrendű lesz.
2. módszer Ábrázolja az adatok grafikonját
-

Keresse meg a változókat, amelyek lineáris függvénnyel reprezentálják a reakciót. A reakciót ábrázoló grafikonról azt állítják, hogy lineáris, ha a növekedési sebessége állandó. Más szavakkal azt jelenti, hogy a függő változó az első másodpercben ugyanolyan mértékben változik, mint a második, harmadik stb. Vizuálisan a vonaldiagram egyenes vonalként jelenik meg az oldalon. -

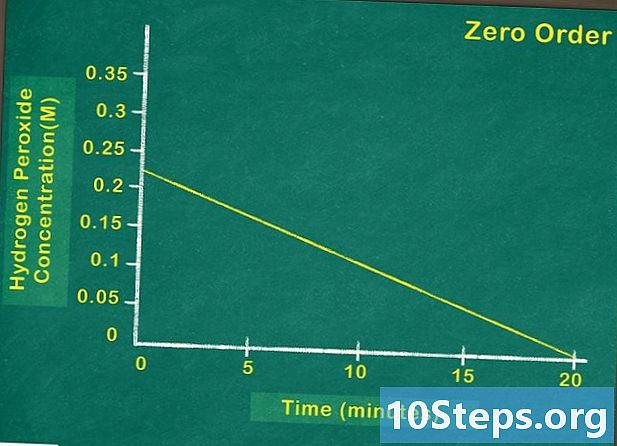
Mutassa be a reagens koncentrációját az idő függvényében. A grafikonon látható a reagens mennyisége, amely a reakció bármely pillanatában fennmarad. Ha a grafikonon ábrázolt funkció lineáris, ez azt jelenti, hogy a reagens koncentrációja nincs hatással a reakció sebességére. Ezért nulla fokozatú reagenssel kell szembenéznie. -
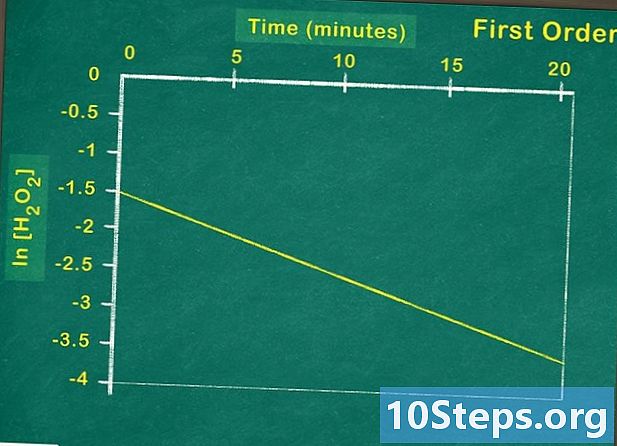
Rajzolja meg a természetes logaritmát. Ha a reagens koncentrációjának természetes logaritmusát az idő függvényében ábrázolja, akkor lineáris függvényt kap, ez azt jelenti, hogy a reagens elsőrendű. Ha nem ez a helyzet, akkor a grafikonon ellenőriznie kell, hogy ez egy második rendű reakció. -

Mutassa be a reagens koncentrációjának inverzét az idő függvényében. Ha a megfelelő függvény egy lineáris függvény, akkor az az oka, hogy egy másodrendű reakcióval van dolgod. Ezért a reakció sebessége négyszögletesen növekszik a reagens koncentrációjának növekedése szempontjából. Ha a talált függvény nem lineáris, az azért van, mert nulla vagy első rendű reakció van. -

Összegezze az összes reagens sorrendjét. Miután minden reagenst létrehozott egy lineáris funkciót, megismerheti az egyes reagensek sorrendjét. Ezután kiszámíthatja az általános rendelést. Csak annyit kell tennie, hogy összeadja a különböző reagensek sorrendjét, hogy megkapja a reakció általános sorrendjét.
3. módszer Kísérletileg oldja meg a problémát
-

Keresse meg az elsőrendű reagenst. Tudja meg, mi a reakció sorrendje, amikor a reakció sebessége megduplázódik, ha az egyik reagens koncentrációja megkétszereződik. Vegye figyelembe, hogy a reagens koncentrációjának megkétszereződése és a reakciósebesség megkétszereződése azt jelenti, hogy a reagens elsőrendű. Ebben az esetben mindkét reagens elsőrendű. Ennélfogva arra a következtetésre juthat, hogy e két elsőrendű reagens összege másodrendű kémiai reakciót vált ki. -

Keresse meg a nulla sorrendű reagenst. Határozza meg a reakció sorrendjét, amelynek során a reakció sebessége nem változik, amikor mindkét reagens koncentrációja megkétszereződik. Ha az egyik reagens koncentrációjának megkétszereződése nem változtatja meg a reakció sebességét, ez azt jelenti, hogy a kérdéses reagens nulla rendű. Ebben az esetben a két reagens nulla rendű. Ha két nulla rendű reagenst keverünk, akkor nulla rendű globális kémiai reakciót kapunk. -

Keresse meg a második rendű reagenst. Keresse meg, mely sorrendű olyan reakció, amelynek sebessége megnégyszereződik, ha az egyik reagens megduplázódik. Az a reagens, amely így befolyásolja a reakció sebességét, másodrendű. A másik reagens ebben az esetben nincs hatással és nulla rendű lesz. E két reagens sorrendének összege kettő, ami azt jelenti, hogy globálisan másodrendű kémiai reakció.