Tartalom
- szakaszában
- 1. módszer Egy egyenlet kiegyensúlyozása próba és hiba módszerrel
- 2. módszer Kiegyenlítse az egyenletet algebrai módszerrel
A kémiában egy egyenlet határozza meg, hogy mi történt a kémiai reakció során. Az egyenlet bal oldalán helyezzük el a kísérlethez használt reagenseket, a jobb oldalon pedig a kísérlet során kapott termékeket. A tömeg megőrzésének (Lavoisier) elve szerint egy kémiai reakció során egyetlen atom sem tűnik el, semmilyen nem keletkezik, eltérően egyesülnek. Összefoglalva: az elem jobb oldalán ugyanazzal a számmal kell rendelkeznie, mint az egyenlet bal oldalán. Ezért kell a kiegyenlítő egyenletet mindig kiegyensúlyozni.
szakaszában
1. módszer Egy egyenlet kiegyensúlyozása próba és hiba módszerrel
-
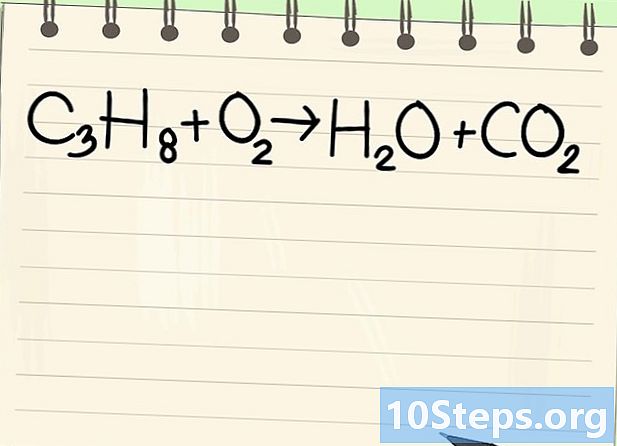
Jegyezzük fel a mérleg egyenletét. A következő egyenletet fogjuk kezelni:- C3H8 + O2 -> H2O + CO2
- Ez a propán égés egyenlete (C3H8) oxigénben: víz és szén-dioxid keletkezik.
-
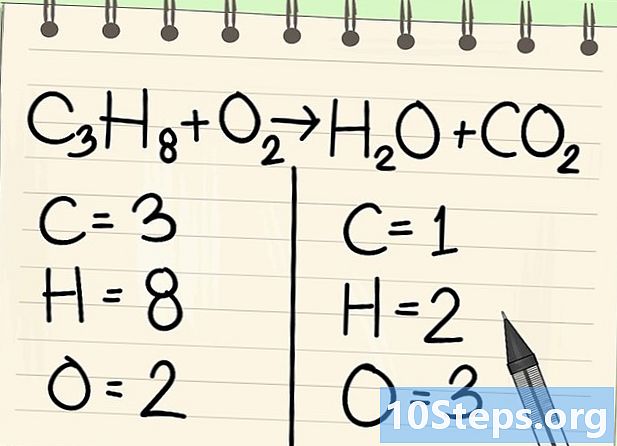
Számolja meg az atomokat. Írja be az egyes elemek adatmezőinek számát az egyenlet egyik oldalára, majd a másikra. Ehhez vegye figyelembe az indexeket, ha nem létezik, akkor az index 1.- A bal oldalon 3 szénatom, 8 hidrogén és 2 oxigén van.
- Jobb oldalon van 1 atom szén, 2 hidrogén és 3 oxigén.
-
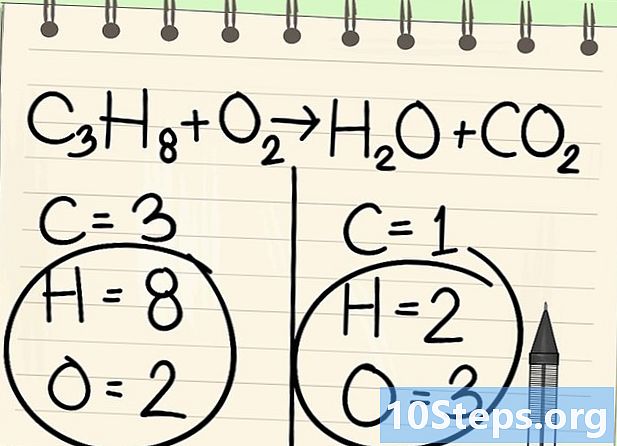
Hagyja félre a hidrogént és az oxigént. -

Kezdje el a kiegyensúlyozást a megfelelő elemmel. Mindig a molekulában lévővel kezdjük a reakció előtt és után. Ha több van, akkor vegye be azt, amelyik az egyik molekula monovalens. Itt kezdjük a szénatomokkal. -

Kiegyensúlyozza a szénatomokat. Adjunk jobbra egy együtthatót a szén-dioxid-molekula (CO2), amelyben a szén latom önmagában van. 3-at teszünk, hogy megkapjuk a 3 bal atomot.- C3H8 + O2 -> H2O + 3CO2
- Tehát jobb oldalon 3 szénatom van a koefficienssel (3CO.)2) és 3 szénatom a bal oldalon, az indexnek köszönhetően (C3H8).
- Egy egyenletben megadhatja az összes kívánt együtthatót, de a nyomokat nem érinti.
-
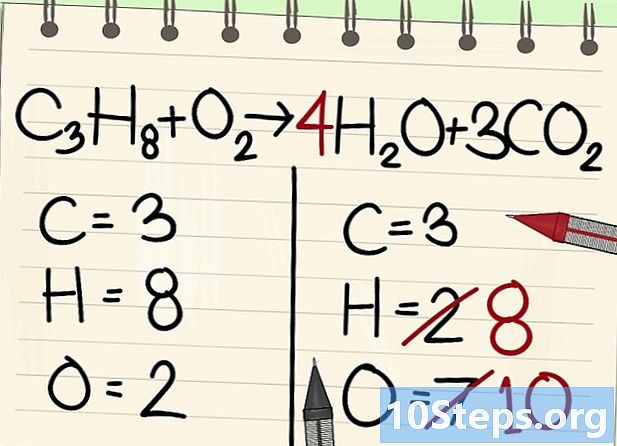
Kiegyensúlyozza a hidrogénatomokat. Mivel nyolc van az egyenletből, annyira jobbra van szükséged.- C3H8 + O2 --> 4H2O + 3CO2
- A jobb oldalon 4-es együtthatót fogsz megadni, mivel a hidrogén bivalens a vízmolekulában: a 2. mutató azt jelzi, hogy két hidrogénatom van társítva.
- A jobb oldalon lévő hidrogénatomok számának megszerzéséhez a 4-es együtthatót szorozni kell a 2-es mutatóval, vagy 8 atommal.
- Ami az oxigénatomokat illeti, jobb oldalon ma már 6 az egyik oldalon, a 3CO három molekulájából származik2 (3 x 2 = 6 atom) és 4 a 4H 4 molekula közül2O (4 x 1 = 4 atom), vagyis összesen 10 atom oxigén.
-
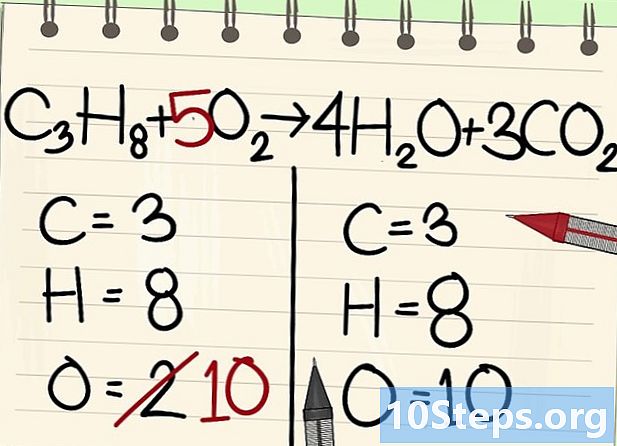
Kiegyensúlyozza az oxigénatomjait.- A szén és a hidrogén egyensúlya miatt az oxigénatomok száma nem egyenlő az egyenlet mindkét oldalán. Korábban láttuk, hogy a jobb oldalon 10 oxigénatom van (4 vízmolekulákból és 6 szén-dioxidmolekulákból). A bal oldalon csak 2 van (O - tól2).
- Az oxigén kiegyensúlyozásához 5-ös együtthatót kell hozzáadni a bal oldali oxigénmolekulához: 10 oxigénatom van a bal oldalon, a másik pedig a jobb oldalon.
- C3H8 + 5O2 -> 4H2O + 3CO2
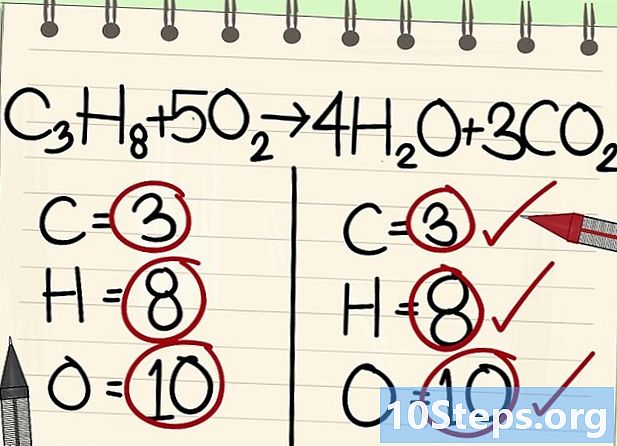
- Minden atom (szén, hidrogén és oxigén) kiegyensúlyozott: egyenlete kiegyensúlyozott.
2. módszer Kiegyenlítse az egyenletet algebrai módszerrel
-

Írja be az egyenletet az egyenlethez. Az egyes molekulákhoz szó szerinti együtthatót rendeljen. Felhívjuk őket van, b, c és d. -
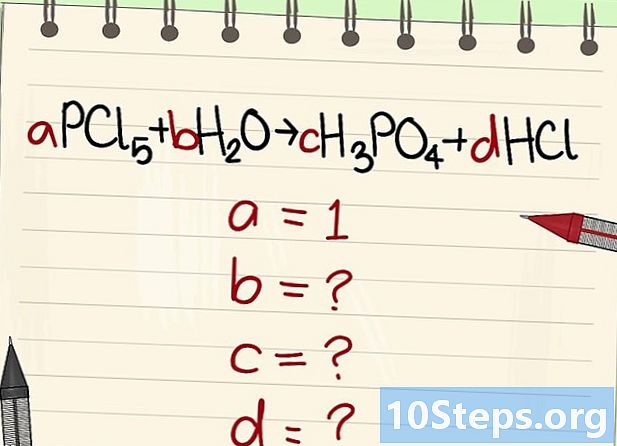
Keresse meg a többi literális együttható értékét. Fel fogjuk kérdezni van = 1. -

Keresse meg az együtthatók közötti összefüggéseket. Balra nézve (reagensek) és jobbra (termékek) nézve állapítsa meg a különbségeket az említett együtthatók között.- Vegyük a következő egyenletet: aPCl5 + bH2O = cH3PO4 + dHCl. Azt állították, hogy a = 1, ami azt jelenti, hogy c = a, d = 5a és 2b = 3c + d. Számítások elvégezve, c = 1, d = 5 és b = 4.

- Vegyük a következő egyenletet: aPCl5 + bH2O = cH3PO4 + dHCl. Azt állították, hogy a = 1, ami azt jelenti, hogy c = a, d = 5a és 2b = 3c + d. Számítások elvégezve, c = 1, d = 5 és b = 4.